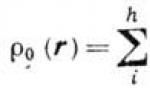Строение кристаллов. Кристаллическое строение металлов. Кристаллическая решетка металлов Существенные характеристики кристаллической структуры кратко
КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА
Расположение атомов, ионов, молекул в кристалле. Кристалл с определ. хим. ф-лой имеет присущую ему К. с., обладающую трёхмерной периодичностью - кристаллической решеткой.
Термин "К. с." употребляют вместо термина "кристаллич. решётка", когда идёт об энергии решётки, динамике решётки, о решётке как конкретной структуре того или иного хим. соединения, об описании атомного строения конкретных соединений и их модификаций. Геом. описание конкретной К. с. состоит в указании координат центров атомов в элементарной ячейке кристалла, что позволяет определять межатомные расстояния и тем самым изучать геом. особенности К. с.
Осн. методами исследования К. с. являются дифракционные - рентгеновский структурный анализ, нейтронография , электронография.
Дифракционные методы дают непрерывное, усреднённое по времени и по всему объёму кристалла рассеивающей материи в элементарной ячейке К. с. Методами рентг. анализа получают электронной плотности в кристалле, к-рое рассчитывается как ряд Фурье:
где х, у, z
- координаты в элементарной ячейке, - её объём, F hkl
- коэф.
Фурье, наз. структурными амплитудами. Распределение электронной плотности в ячейке можно приближённо представить как сумму электронных плотностей атомов (r i
):

где i
- усреднённые во времени, т. е. размазанные тепловым движением, распределения электронов в атоме. Максимумы (1) соответствуют атомам - сгусткам электронной плотности, что позволяет найти координаты их центров r
( х, у, z
) и создать геом. модель, установив межатомные расстояния с точностью до 0,0001 - 0,00001 нм.
В нейтронографии аналогично (1) по амплитудам ядерного рассеяния кристалла F
нейтр определяют распределение ядерной плотности п(r
)ячейки, т. е. вероятностное, размазанное тепловым движением распределение ядер (см. Нейтронография структурная).
При наличии у атомов магн. момента нейтронографически определяют магн. К. с.- распределение спиновой плотности (см. Магнитная ).
В электронографии по амплитудам F эл
согласно (1) определяют распределение электростатич. (суммарного - ядер и электронов) потенциала (r).
Положение максимумов всех трёх распределений совпадает - это и есть среднее во времени положение центров атомов (ядер) в элементарной ячейке.
Геометрическая модель.
Для создания геом. модели К. с. необходимо: знание параметров элементарной ячейки (параллелепипеда повторяемости) структуры - в общем случае длин её рёбер а, Ь, с
и углов ; указание симметрии К. с., т. е. принадлежности её к одной из 230 пространственных групп (см. Симметрия кристаллов
)и тем самым - типу Браве решётки
;.
указание координат всех химически различных атомов и симметрии их позиций. Для этого достаточно знать координаты атомов в симметрически независимой части ячейки, из к-рых можно с учётом операций пространственной группы вывести положение всех атомов К. с. На этой основе рассчитываются межатомные расстояния, взаимная координация атомов и др. геом. характеристики К. с. Графически К. с. изображают расположением атомов ("шариков") в элементарной ячейке (рис. 1, а). Крупными соприкасающимися "шарами" в случае необходимости можно показать контакты атомов в плотноупакованных неорганич. (рис. 1, б
)или молекулярных структурах. Для изображения ионных К. с. часто пользуются полиэдрами, в вершинах к-рых находятся анионы, в центрах - катионы (рис. 1, в).
Геом. анализ К. с. позволил развить целый ряд обобщений и законов атомной структуры кристаллов- представления об атомных радиусах, о типах хим. связи в кристаллах (ионной, ковалентной, металлической, ван-дер-ваальсовой, водородной), правила плотнейшей упаковки атомов и молекул в К. с., связи К. с. со свойствами кристаллов (см. Кристаллохимия).
Анализ К. с. и её симметрии служит отправным пунктом расчётов энергетич. спектра, истолкования физ. свойств кристалла (см. Кристаллофизика).
Параметры элементарных ячеек некоторых кристаллов
| Типы кристаллов | Периоды элементарной ячейки, нм | Число атомов в элементарной ячейке | ||
| Неорганические и простые молекулярные соединения | до сотен | |||
| Сложные органические соединения | до тысяч | |||
| Вирусы | ||||
Изучено более 100 тыс. К. с. разл. веществ, из них ок. 20 тыс. неорганич. К. с. элементов, разл. соединений, минералов, остальную - большую часть - составляют органич. К. с. Периоды решётки разл. кристаллов составляют от долей до сотен нм (табл.). Рентге-ноструктурный анализ К. с. органич. соединений есть наиб. точный и достоверный метод определения пространственного и хим. строения составляющих их молекул. Изучено неск. сотен К. с. сложнейших веществ биол. происхождения: белков, нуклеиновых кислот, вирусов (см. Биологический кристалл).
Существуют международные ЭВМ-банки данных, описывающие все неорганич., органич. и биологич. К. с.

Рис. 1. Модели кристаллических структур: а
- алмаз, б -
хлористый NaCl, в
- бафертисит BaFe 2 Tl (Si 2 O 7)O(OH).
Совр. прецизионные дифракционные методы позволяют, кроме координат атомов (геом. модели), определять др. характеристики К. с.
Экспериментально можно детально определить ан-гармонизм тепловых колебаний атомов К. с., описываемый тензорами более высокого ранга. Поверхность, характеризующая колебания, уже не является трёхосным гауссовым эллипсоидом и не имеет центра симметрии. Параметры энгармонизма позволяют связать характер колебаний атомов с акустич., сегнетоэлектрич. свойствами кристаллов, указать возможные смещения атомов при фазовых переходах в высокотемпературные модификации К. с. Частоты колебаний атомов в К. с. составляют порядка 10 12 Гц, их определяют спектроскопич. методами, методом неупругого рассеяния нейтронов (см. Колебания кристаллической решётки).

Рис. 2. Эллипсоиды тепловых колебаний атомов в решётке: а - общий случай произвольной ориентации; б - анизотропия колебаний в структуре, - ацетилена - bis-циклопентадиена никеля при З00 К. Слева - ацетилена, справа - циклопентадиена.
Вычитая из наблюдаемого распределения (r
)(1) распределение (r
)(2), можно найти деформационную электронную кристаллической структуры.
Дело в том, что выражение (2) является суммой свободных "проатомов" К. с., размазанных тепловым движением, электронная плотность к-рых не изменена вследствие образования хим. связи в К. с., а выражение (1) соответствует электронной плотности кристалла, в к-рой все эти связи образовались. Несмотря на то, что значения невелики, они позволяют выявить ряд тонких деталей К. с. (рис. 3). Так, появление максимума на месте "проатома" показывает на излишек электронов в нём, т. е. что этот заряжен отрицательно, т. к. является анионом, а появление минимума - что он является катионом; по величине dr деф можно оценить степень ионизации. В ионных К. с. электроны перераспределяются между атомами, но в "межатомном пространстве" практически =0. В металлич. К. с. часть электронов атомов обобществлена и образует равномерную электронную плотность межатомного пространства. В ковалентных кристаллах отчётливо выявляет пики между атомами, соответствующие парам электронов, образующих ковалентную связь. В молекулярных кристаллах фиксируются пики , соответствующие неподелённым электронным парам атомов (рис. 3). Математич. обработка (r
)и позволяет находить распределение электростатич. потенциала электронов, потенциальную энергию, градиент поля на атомах и т. п. С помощью электронографии можно находить суммарный (ядер и электронов) деформац. атомов и определять их .

Рис. 3. Деформационная электронная плотность циануровой кислоты. Пики на связях - валентные связывающие электроны, около атома О - неподелённая электронная пара.
Дефекты. К. с., в к-рой все позиции заполнены атомами, наз. идеальной К. с. Однако в действительности К. с. имеет ряд дефектов - точечных (смещения атомов из идеальных позиций, замещение этих атомов атомами примеси, вакансии, атомы внедрения и т. п.), линейных и двумерных (дислокации , ошибки в наложении слоев и т. п.) (см. Дефекты
в кристаллах). Если количество точечных дефектов велико, можно фиксировать среднее по всем ячейкам изменение бр электронной плотности К. с., напр. в рубине А1 2 0 3 +0,05% Сr, где Сг замещает позиции А1. В структурах твёрдых растворов вычитания или внедрения анализ бр даёт сведения о заселённости атомами тех или иных позиций.
Наряду с кристаллич. веществами, в к-рых атомы колеблются около фиксиров. положений равновесия, существуют кристаллы, в к-рых отд. атомы, их группировки или целые молекулы статистически занимают разл. положения (см. Твёрдые ).
Тепловое молекул в нек-рых кристаллич. структурах таково, что при сохранении положения центра тяжести они могут быть в состоянии сферич. или цилиндрич. вращения. В нек-рых кристаллах при наличии жёсткого трёхмерно-периодич. каркаса структуры из одних атомов нек-рые ионы могут свободно мигрировать, перетекать по каналам каркаса (см. Ионные суперпроводники).
Пути миграции заряженных ионог фиксируются распределением dr деф. Аналогично в каркасных К. с., напр. цеолитах, внутри пустот могут находиться молекулы органич. веществ, также фиксируемые по dr.

Рис. 4. Электронно-микроскопическое изображение атомной структуры кластера фосфора в кремнии.
Конкретное расположение дефектов в реальной К. с. исследуется также методами рентгеновской и нейтронной топографии, электронной микроскопии (рис. 4) и др.
Сложные К. с.
Наряду с идеальными трёхмернопериодич. К. с. существуют др. типы кристаллич. упорядоченности атомов. Так, в сверхструктурах на "фоне" правильной трёхмерной решётки наблюдается дополнит. упорядоченность с периодами, кратными одномуили двум периодам идеальной К. с., обязанная, напр., распределению магн. моментов атомов, электрич. диполей и т. п. Иногда период такой сверхструктуры не кратен периоду основной решётки, и тогда К. с. наз. несоразмерной. К. с. с периодическими в к.-л. направлении включениями инородных атомов наз. модулированными. Искусственно приготовляемые в микроэлектронике гетероструктуры, напр. AlAs-GaAs, имеют общую, одну и ту же кристаллич. решётку (в смысле равенства периодов), но в них чередуются слои то одного, то другого состава (рис. 5). Существуют К. с. (напр., слоистые силикаты) с неупорядоченным наложением двух пли более сортов слоев фиксиров. строения, напр. структуры из сочленённых "лент" или "колонок" фиксиров. состава. Всё это - фактически когерентное сцепление в едином кристалле на атомном уровне микроучастков разл. К. с.

Рис. 5. Электронная микрофотография расположения атомов в гетероструктуре AlAs-GaAs (увеличение 10 6).
Более сложные нарушения упорядоченности, приводящие к частичной или полной потере осн. признака К. с.- дальнего порядка (см. Дальний и ближний порядок),
наблюдаются в структуре полимеров, жидких кристаллов, квазикристаллов.
К. с. конкретных веществ классифицируются по симметрии и тину хим. связей. Многие вещества разного хим. состава, но с одинаковым соотношением числа атомов имеют геометрически подобные К. с., что наз. из о структурностью (напр., MgO и TiN - структурный тип NaCl). Из симметрии К. с. можно предсказать возможные в данном кристалле физ. свойства. Количественные характеристики разных свойств, например упругих, оптических, электрических и т. п., можно увязать с конкретным расположением атомов в К. с., а иногда и прямо рассчитать из К. с. (см. Кристаллы),
Лит.: Structure reports. Publ. for the Intern. Union of Crystallography, Utrecht, 1951-87 - ; Molecular structures and dimensions. Bibliography, ed. by O. Kennard and D. Watson, v. 1-15, Utrecht, 1971-84; Современная , т. 2, M., 1979; Нейтроны и твердое тело, т. 2, М., 1981; Вайнштейн Б. К., Структурная классификация состояний вещества, в кн.: Кристаллография и кристаллохимия, М., 1986; Уоллс А., Структурная неорганическая химия, пер. с англ., т. 1, М., 1987. Б. К . Вайнштейн.
Физическая энциклопедия. В 5-ти томах. - М.: Советская энциклопедия . Главный редактор А. М. Прохоров . 1988 .
Наиболее обширной группой кристаллов являются тела, построенные из молекул. Достаточно представителей имеют и ионные соединения. В этих случаях, как мы уже говорили, представление о кристалле как о плотно уложенных частицах вполне оправдано. Однако необходимо остановиться на тех структурах, где направленности связей между атомами, отклонение электронного облака от сферической симметрии и прочее являются причиной образования структур, которые не могут уже рассматриваться столь просто.
К таким исключениям принадлежат структуры атомов, связанных общими электронами.
У большого числа металлов наблюдаются структуры с объемно-центрированной кубической ячейкой. В этих кристаллах каждый атом будет иметь восемь соседей, а не двенадцать, как в плотнейшей упаковке шаров. Так ведут себя, например, атомы железа (рис. 257). Решетка железа - кубическая; атомы железа расположены в вершинах и центрах кубов. Такой же структурой обладают литий, калий, цезий и ряд других веществ.
На рис. 263 структура кристаллической ртути сравнивается с идеальной кубической плотнейшей упаковкой. Легко видеть, что характер расположения центров атомов одинаков, но в структуре
ртути расстояния между слоями уменьшились, а расстояния между атомами одного слоя возросли, как будто бы мы плотно упаковали слегка сплющенные шары.
Примеров таких в большей или меньшей степени «испорченных» шготнейших упаковок очень много. Например, в случае льда (рис. 264) родство с шаровой упаковкой теряется полностью. Связь между каждой парой атомов кислорода осуществляется одним атомом водорода. В этих четырех связях каждый атом водорода приходится на два атома кислорода - противоречия с химической формулой воды изображенная на рис. 264 структура, конечно, не имеет. Для наглядности «водородная» связь на рисунке изображена в виде «перешейка». Структура льда очень рыхлая, на рисунке заметны большие «дыры». Если мысленно продолжить структуру над плоскостью чертежа, то эти дыры превратятся в широкие каналы, пронизывающие структуру.


Структура льда - важное исключение из общего правила. Это не значит, что редкими являются случаи, когда уподобление кристалла плотной упаковке частиц теряет свой смысл.
Как мы уже говорили выше, полностью теряется аналогия с плотной упаковкой шаров в случае кристаллов, построенных из атомов, связанных общими электронами.
Структура сульфида цинка, показанная выше на рис. 257, очень характерна. Так же выглядят и структуры некоторых элементов: углерода (алмаз), кремния, германия, олова (белого).
Возможны случаи, когда гомеополярные связи образуют слои и цепи атомов.
На рис. 265 изображена структура графита. Атомы углерода в графите образуют слоевую структуру. Но это не слои плотнейшей упаковки. Построить слой графита из соприкасающихся сфер нельзя. У графита слои сильно связанных атомов - плоские. Мышьяк и фосфор также дают слоистые в этом смысле структуры, но атомы слоя расположены не в одной плоскости. В качестве примера
структуры, состоящей из цепочек сильносвязанных атомов, можно привести серый селен. Каждый атом этого вещества крепко связан лишь с двумя соседями. У серого селена атомы образуют бесконечную спираль, навивающуюся на прямую линию. Расстояния между атомами соседних спиралей значительно больше расстояния между ближайшими атомами, входящими в одну и ту же спираль.
Черный матовый мягкий графит, которым мы пишем, и блестящий прозрачный твердый, режущий стекло алмаз построены из одних и тех же атомов - из атомов углерода. На этом примере с исключительной отчетливостью видно, как резко определяются свойства кристаллов взаимным расположением атомов. Из графита делают огнеупорные тигли, выдерживающие температуру до 2000-3000 °С, а алмаз горит при температуре выше 700 °С; удельный вес алмаза 3,5, а графита 2,1; графит проводит электрический ток, алмаз - нет, и т. д.
Эта особенность образовывать разные кристаллы присуща не только одному углероду. Почти каждый химический элемент в кристаллическом состоянии и любое вещество существуют в нескольких разновидностях. Нам известно шесть разновидностей льда, девять разновидностей серы, четыре разновидности железа.
При комнатной температуре атомы железа образуют кубическую решетку, в которой атомы занимают места по вершинам и в центре кубов; каждый атом имеет восемь соседей. При высокой температуре атомы железа образуют плотнейшую упаковку: каждый атом имеет двенадцать соседей. Железо с числом соседей восемь - мягкое, железо с числом соседей двенадцать - твердое. Закалка стали фиксирует при комнатной температуре плотнейшую кубическую упаковку, устойчивую при более высоких температурах.
Уже из примеров углерода и железа видно, что разновидности кристаллов одного и того же вещества совершенно не похожи друг на друга по структуре. То же относится и к другим веществам.
Так, например, желтая сера образует в кристалле гофрированные кольца из восьми атомов. Иначе говоря, в кристалле видна молекула серы из восьми атомов. Красная сера тоже состоит из таких колец, однако повернуты они друг к другу совсем иначе.
Желтый фосфор дает кубическую структуру с числом ближайших соседей, равным восьми. Черный фосфор - слоистая структура типа графита.
Серое олово имеет структуру такую же, как алмаз. Белое олово можно мысленно получить из серого, если сильно сжать алмазную структуру вдоль оси куба. В результате этого сплющивания число ближайших соседей у атома олова становится равным шести вместо четырех.
У органических веществ также часто встречаются кристаллические разновидности. Те же самые молекулы располагаются по-разному одна по отношению к другой.

В зависимости от вида структурных единиц вещества различают каркасные (атомные), металлические, ионные и молекулярные структуры. Встречаются и комбинированные типы структур.
В каркасной структуре атомы одного или нескольких химических элементов связаны ковалентными химическими связями. Вследствие этого выбор определенной структуры диктуется направленностью связей. В структуре отсутствуют изолированные группы атомов, т.е. сетка ковалентных связей охватывает всю структуру. Наиболее известным примером вещества с каркасной структурой является алмаз. Элементарная ячейка алмаза представлена на рис. 8.7. Атомы углерода расположены в вершинах кубической ячейки, центрах всех граней и в шахматном порядке занимают центры четырех из восьми кубиков, на которые можно разбить элементарную ячейку. От этих атомов внутри ячейки ковалентные связи тетраэ- дрически направлены к атому углерода в одной из вершин и трем атомам углерода на гранях. Расстояния между всеми атомами углерода 154 пм. Алмазоподобные структуры имеют многие вещества. Среди них кремний, карбид кремния SiC, сульфид цинка (цинковая обманка) ZnS. В этом веществе атомы цинка находятся в вершинах и на гранях элементарной ячейки, а атомы серы занимают места внутри ячейки. Таким образом, структура этого вещества, по традиции причисляемого к солям, не ионная, а каркасная.
Кристалл вещества с каркасной структурой может рассматриваться как единая молекула. Такие вещества проявляют термическую устойчивость, практически не растворимы в воде, имеют высокие температуры плавления и твердость.
Металлическая структура отличается от каркасной тем, что расположение атомов определяется не направленностью связей, а только условием плотнейшей упаковки атомных сфер. Для большинства металлов характерны лишь три разновидности элементарных ячеек - объемно-центрированная кубическая, гранецентрированная кубическая и гексагональная компактная. Многие металлы проявляют полиморфизм , изменяя кристаллическую структуру при нагревании.
Рис. 8.7.
в виде клиньев показаны связи между атомами углерода внутри ячейки
Ионная структура строится из чередующихся ионов с противоположными по знаку зарядами. Такого типа структуру имеет хлорид натрия (см. рис. 2.8). Положения ионов натрия и хлора полностью взаимозаменяемы. В вершинах ячейки и центрах граней можно поместить ионы хлора. Тогда ионы натрия окажутся на серединах ребер и в центре ячейки. Можно поступить наоборот, т.е. все ионы поменять местами. Такую структуру можно представить как две гранецентрированные решетки - одна с ионами Na + и другая с ионами С1~, - вставленные одна в другую со смещением на половину длины ребра куба.
Возникновение той или иной ионной структуры зависит главным образом от зарядов ионов и соотношения их радиусов. В хлориде цезия, более тяжелого щелочного металла, чем натрий, значительно увеличен радиус катиона, вследствие чего его координационное число повышается до восьми. В кубической ячейке каждый ион цезия окружен восемью ионами хлора (рис. 8.8). Эту структуру тоже можно представить как две кубические решетки, образованные ионами цезия и ионами хлора, вставленные одна в другую так, что ион одного вида оказывается в центре ячейки с ионами другого вида.

Рис. 8.8.
Вещества с ионной структурой характеризуются высокими температурами плавления вследствие значительной энергии электростатического притяжения ионов. Многие ионные вещества хорошо растворимы в воде.
Вещества с молекулярными структурами резко отличаются от рассмотренных выше низкими температурами плавления. Именно среди них имеются жидкости и газы. При рентгеноструктурном исследовании таких веществ обнаруживаются короткие межатомные расстояния внутри молекул и значительно удлиненные расстояния между такими же атомами в разных молекулах. Например, в кристаллах иода 1 2 (рис. 8.9) расстояние между атомами в молекуле - 272 пм, расстояние между молекулами в слое - 350 нм, а ближайшее расстояние между атомами, находящимися в разных слоях, - 397 пм.

Рис . 8.9.
Вещества, состоящие из многоатомных молекул, образуют весьма сложные структуры. Без рентгеновского исследования понять их строение было бы просто невозможно. Можно напомнить о молекулах ДНК, имеющих двойную спиральную структуру. Определение их структуры открыло новый этап в развитии биологии.
Очевидно, что молекула не может находиться в узле кристаллической структуры, так как представляет собой некоторую совокупность атомов. На рис. 8.10 в качестве примера приведена структура комплексного соединения |Pt(CN) 2 (NH 3)(NH 2 CH 3)|. Элементарная ячейка представлена в виде проекции вдоль оси У. Вершины ячейки не заняты атомами. Плоские молекулы комплексного соединения на проекции видны сбоку. Пунктиром показаны водородные связи между молекулами аммиака, находящимися в разных молекулах комплексного соединения. Оси симметрии второго порядка проходят параллельно оси У. Одна из них проходит через центр ячейки. Восемь молекул, находящихся в элементарной ячейке, располагаются на двух уровнях по оси У в шахматном порядке. Этот пример дает представление о сложности молекулярных структур.

Рис. 8.10. Проекция элементарной ячейки комплексного соединения вдоль оси Y
Молекул в кристалле. Кристаллическая структура определяется кристаллической решёткой, симметрией кристалла, формой и размерами его элементарной ячейки, типом и координатами атомов в ячейке. В идеальном кристалле содержание и положения атомов во всех ячейках одинаковые. За исключением химического состава все остальные характеристики кристаллической структуры определяются дифракционными методами - рентгеновского структурного анализа, электронографии, нейтронографии структурной. В кристаллах твёрдых растворов и при других отклонениях химического состава от стехиометрии структурный анализ высокой точности позволяет определить и уточнить соответствующие параметры.
При падении на монокристалл излучения с длиной волны порядка межатомных расстояний возникает дифракционная картина, которая состоит из дискретного набора пиков. Положения пиков определяются кристаллической решёткой, а их интенсивности зависят от типа атомов и их расположения в элементарной ячейке кристалла. Наличие в кристалле элементов симметрии проявляется в равенстве интенсивностей соответствующих пиков. Исключение составляет то, что дифракционная картина всегда центросимметрична (независимо от наличия или отсутствия центра симметрии в кристалле). Вследствие этого с помощью рентгеноструктурного анализа можно различить только 122 группы из 230 пространственных (фёдоровских) групп симметрии кристаллов. Наличие (или отсутствие) центра симметрии в кристалле можно установить по статистике распределения интенсивностей дифракционных пиков. Экспериментальное определение отсутствия центра симметрии возможно, если в кристалле есть атомы с аномальным рассеянием используемого излучения. Наиболее сложной является методика определения координат атомов в элементарной ячейке кристалла.
Рассмотрим кристаллическую структуру некоторых элементов периодической системы. Так, в двух модификациях полония различной симметрии содержится по 1 атому в элементарной ячейке. В элементарных ячейках кристаллов калия, цинка, молибдена и ряда других элементов содержится по 2 атома, в ячейке теллура - 3, а в двух модификациях марганца по 20 и 58 атомов в ячейке соответственно. В кристаллах неорганических и органических соединений могут находиться от единиц до сотен атомов в ячейке. В кристаллах белков от тысяч до сотни тысяч атомов, а в закристаллизованных вирусах ещё на 2-3 порядка больше.
 Рассмотрим кристаллическую структуру кристаллов различной природы. Кристаллы ниобата лития LiNbO 3 широко применяются в лазерной технике и оптике. На рисунке 1 представлены два изображения его кристаллической структуры. В первом случае атомы - шарики. Крупные анионы кислорода не позволяют увидеть общую организацию строения кристалла. Л. Полинг предложил изображать неорганические структуры в форме полиэдров, вершины которых являются центрами анионов, а внутри полиэдров находится соответствующий катион. В представленном на рисунке 1, б ниобате лития это октаэдры и .
Рассмотрим кристаллическую структуру кристаллов различной природы. Кристаллы ниобата лития LiNbO 3 широко применяются в лазерной технике и оптике. На рисунке 1 представлены два изображения его кристаллической структуры. В первом случае атомы - шарики. Крупные анионы кислорода не позволяют увидеть общую организацию строения кристалла. Л. Полинг предложил изображать неорганические структуры в форме полиэдров, вершины которых являются центрами анионов, а внутри полиэдров находится соответствующий катион. В представленном на рисунке 1, б ниобате лития это октаэдры и .
Кристаллы семейства ниобата стронция-бария Sr 1-x Ba x Nb 2 О 6 характеризуются нелинейными оптическими, пиро и пьезоэлектрическими свойствами (смотри Пироэлектрики, Пьезоэлектричество), которыми можно целенаправленно управлять, меняя соотношение стронция и бария. На рисунке 2 представлена кристаллическая структура этих кристаллов, из которой видно, что часть атомов стронция занимает собственную позицию, а в другой позиции статистически расположены атомы бария и стронция, координаты которых несколько различаются.
 Кристаллические структуры органических соединений обычно представляют собой плотную упаковку молекул, связанных слабыми ван-дер-ваальсовыми и, возможно, водородными связями. Кристаллы органических соединений находят применение в технике, однако часто их получают только для того, чтобы рентгеновскими методами установить атомное строение молекул, так как органические соединения в растворах (а биологически активные соединения в организме) действуют в качестве отдельных молекул. Структуры молекул антибиотиков - аналогов энниатина В и споридесмолида представлены на рисунке 3. Первое соединение является препаратом для избирательного транспорта катионов через биологические мембраны, а второе - лишено этого свойства из-за внутримолекулярных водородных связей, хотя обе молекулы циклические и состоят из 6 аминокислотных остатков. Различие в строении молекул установлено по кристаллической структуре соответствующих кристаллов.
Кристаллические структуры органических соединений обычно представляют собой плотную упаковку молекул, связанных слабыми ван-дер-ваальсовыми и, возможно, водородными связями. Кристаллы органических соединений находят применение в технике, однако часто их получают только для того, чтобы рентгеновскими методами установить атомное строение молекул, так как органические соединения в растворах (а биологически активные соединения в организме) действуют в качестве отдельных молекул. Структуры молекул антибиотиков - аналогов энниатина В и споридесмолида представлены на рисунке 3. Первое соединение является препаратом для избирательного транспорта катионов через биологические мембраны, а второе - лишено этого свойства из-за внутримолекулярных водородных связей, хотя обе молекулы циклические и состоят из 6 аминокислотных остатков. Различие в строении молекул установлено по кристаллической структуре соответствующих кристаллов.
Современный структурный анализ высокой точности позволяет определять не только координаты атомов, но и параметры тепловых колебаний атомов с учётом анизотропии и ангармонизма этих колебаний. Для не очень сложных соединений рентгеноструктурным анализом можно установить распределение электронной плотности в их кристаллах. Структурные методы чувствительны к нарушению стехиометрии химического состава кристалла и к его всевозможным дефектам. Обширный материал о структурах кристаллических веществ представлен в электронных базах данных (смотри Кристаллохимия).
Лит.: Белов Н. В. Структура ионных кристаллов и металлических фаз. М., 1947; он же. Структурная кристаллография. М., 1951; Китайгородский А. И. Органическая кристаллохимия. М., 1947; Федоров Е. С. Симметрия и структура кристаллов. М.; Л., 1949; Бландел Т., Джонсон Л. Кристаллография белка. М., 1979.
Изложенное выше позволяет дать следующее определение понятию «кристаллическая структура». Кристаллическая структура – это такая структура, которой свойственно упорядоченное расположение частиц в строго определенных точках пространства, которые образуют кристаллическую решетку. Эта упорядоченность позволяет экспериментально и теоретически полностью изучить структуру твердого состояния и явления, связанные с природой сил взаимодействия в кристаллических телах.
Для каждого кристалла характерна анизотропность и резко выраженная температура перехода в жидкое состояние. Кристаллы характеризуются внешней симметрией в расположении частиц, которая выражается наличием трех элементов симметрии: центра, оси и плоскости симметрии. Центр симметрии – точка, делящая пополам все соединительные между внешними поверхностями кристалла прямые линии, проведенные через нее по любому направлению. Плоскость симметрии делит кристалл на две части, относящиеся друг к другу, как предмет к своему зеркальному отражению. Ось симметрии – это такая линия, при повороте вокруг которой на определенный угол получается полное совпадение нового положения с прежним. Чем больше элементов симметрии, тем выше внешняя симметрия кристалла. Идеально симметричной фигурой является шар.
В настоящее время все многообразие кристаллических форм по сочетанию элементов симметрии (сингонии) сводится к семи типам: правильная (кубическая), тригональная, гексагональная, тетрагональная, ромбическая, моноклинная и триклинная. В таблице 3.2. приведена классификация кристаллов по сингонии.
Таблица 3.2. Классификация кристаллов по сингонии
Кристаллы низшей сингонии характеризуются меньшей симметрией; кристаллы более высокой категории сингонии имеют более совершенную форму кристаллической решетки и, следовательно, являются более устойчивыми в определенных условиях существования.
Многим веществам в кристаллическом состоянии характерен полиморфизм , т.е. способность вещества существовать в виде нескольких кристаллических структур с различными свойствами. Полиморфизм простых веществ называется аллотропией . Известны полиморфные модификации углерода (алмаз, графит), кварца (α-кварц, β-кварц), железа, вольфрама и др.
Если два разных вещества имеют одинаковую кристаллическую структуру, похожую химическую формулу и не очень сильно различаются по размеру составляющих их частиц, то они могут образовывать смешанные кристаллы. Такие вещества называют изоморфными, их способность образовывать смешанные кристаллы – изоморфизмом. Пример: сходные по составу и структуре, но разные по свойствам являются кристаллы каолинита Al 2 O 3 . 2SiO 2 . 2H 2 O, пирофиллита Al 2 O 3 . 4SiO 2 . 2H 2 O и монтмориллонита Al 2 O 3 . 4SiO 2 . 3H 2 O.
Реальные кристаллы. В свей практической деятельности мы имеем дело с реальными кристаллми, которые отличаются от идеальных нарушениями (дефектами) кристаллической решетки, образующимися в результате изменения равновесных условий роста кристаллов, захвата примесей при кристаллизации, а также под влиянием различного рода внешних воздействий.
Аморфная структура
Аморфная структура является одним из физических состояний твердых тел, Аморфные вещества характеризуются двумя особенностями. Во-первых, свойства таких веществ при обычных условиях не зависят от выбранного направления, т.е. они - изотропны . Во-вторых, при повышении температуры происходит размягчение аморфного вещества и постепенный переход его в жидкое состояние. Точное значение температуры плавления отсутствует.
Общим для кристаллического и аморфного состояний веществ является отсутствие поступательного перемещения частиц и сохранение только их колебательного движения около положения равновесия. Различие между ними состоит в наличии геометрически правильной решетки у кристаллов и отсутствии дальнего порядка в расположении атомов у аморфных веществ.
Аморфное состояние вещества, по сравнению с кристаллическим, всегда менее устойчиво и обладает избыточным запасом внутренней энергии. В связи с этим, при определенных условиях, самопроизвольно осуществляется переход из аморфного состояние в кристаллическое.
Твердые тела в аморфном состоянии можно получить двумя путями. Первый путь – быстрое охлаждение расплавов кристаллических веществ, преимущественно ионного и ковалентного строения. Типичный представитель таких аморфных тел – силикатные стекла, битумы, смолы и пр.
Второй путь – диспергация кристаллических структур. В результате диспергации кристаллических тел образуются аморфизованные дисперсии в виде коллоидов и растворов. Разрушаясь или конденсируясь, дисперсии изменяют свое агрегатное состояние. Пересыщенные растворы, например, могут превратиться в гель и образовать полимер или кристаллизоваться.
Аморфные вещества подразделяют на витроиды (стекла), дисперсные системы и полимеры.
Витроиды – это твердые тела в аморфном состоянии, имеющие стекловидную структуру. Как уже отмечалось, стекла образуются в результате быстрого охлаждения, преимущественно силикатных расплавов. Быстрое охлаждение препятствует созданию упорядоченной структуры. Особенно, если молекулы громоздки, а скорость охлаждения велика.